Конечная квантовая теория. ч.2 химические свойства элементов.
В хорошей теории строения атомов вид элемента зависит от количества протонов в нём, а его химические особенности от заполненности электронами внешних электронных орбиталей.
Из-за чего атом имеет форму шара.
На элементарные частицы в атоме действует сила поверхностного натяжения. Вылетающие из атома частицы, сглаживают давление на поверхности атома. Это давление придаёт атому форму сферы.
Подобно действию силы Архимеда, выталкивающему загружённый в воду предмет.
Разглядим строение атома исходя из правил ККТ. Для этого определим радиус шара — сгустка элементарных частиц.
Формула количества шара:
V=4/3*pi*r^3.
Из этого находим радиус атома.
r=((3/(4*pi))*V)^1/3, где r- радиус атома, pi=3,147…, V-количество шара.
Так как мы не знаем количество шара атома совершенно верно, мы воспользуемся для расчётов массой атомов, каковые экспериментально взяты и широко применяются в химии.
m=R*V, где m-ядерная масса. R — (Ро) плотность шара, V-количество шара.
Плотность элементарных частиц при однообразной температуре однообразна и определяется их кинетической энергией. Плотностью возможно пренебречь и принять, что M=V..
Итак r=((3/(4*pi))*M)^1/3,
Подставим молярные веса атомов и возьмём следующие радиусы атомов:
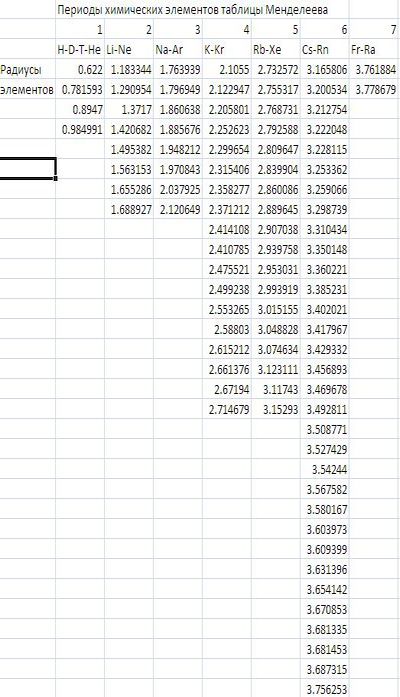
Графически в масштабе разрез атома по слоям Любой круг — внешняя граница атомов в соответствии с таблицей Менделеева:
Атомы отличаются между собой соизмеримыми между собой слоями. Количество слоёв атомов и определяет вид химического элемента.
Химическая реакция.
Химическая реакция это объединение различных атомов в единую структуру. Она происходит следующим образом. Два атома соударяются, наряду с этим имеется пара вариантов развития этого соударения:
1) Они смогут оттолкнуться, в случае если их скорости громадны и нет демпфирующего слоя элементарных частиц на поверхности атомов либо его не хватает чтобы смягчить удар и объединить 2 молекулы в неспециализированную структуру. Инертные газы хороший пример для того чтобы сотрудничества.
2) Они смогут слиться в одно ядро (термоядерный синтез). Это происходит в случае если их скорости очень громадны и смогут превзойти обоюдное отталкивание двух соударяющихся тел (другими словами обоюдное соударение всех элементарных частиц в плоскости их контакта). Наряду с этим сила противодействия пропорциональна площади соприкосновения двух атомов.
S=pi*R^2 и квадратично возрастает от края атома к центру, при деформации и сближении атомов. Кроме этого из этого геометрического правила возможно сделать вывод, что для объединения 2 более тяжёлых атомов в один требуется намного большая энергия, пропорциональная квадрату радиуса атомов.
Поясню. Для объединения 2 атомов несложного водорода требуется E=Rводорода^2=0,62^2=0,38, то для объединения двух атомов Цезия в один атом потребуется уже E=Rцезий^2(1,18^2)=3,16^2=10.
Другими словами для начала термоядерной реакции с объединением 2 атомов Цезия требуется в 26 раза больше энергии (10/0,38), чем для такой же реакции с объединением 2 атомов водорода.
3) Атомы смогут состыковаться и образовать сложное соединение, к примеру H2О, в случае если их внешние слои смягчат удар и примут на себя энергию атомов, не разрешив им оттолкнуться друг от друга. Наряду с этим никакого слияния в единое целое не будет. Атомы рядом, будут иметь какую-то площадь контакта, как мыльные пузыри объединяются в неспециализированные структуры, но сохранят число частиц и свою форму.
Смогут быть уничтожены при нагреве либо другом действии на них.
На протяжении удара происходит следующее:
1) Часть элементарных частиц атомов расходятся в стороны в атома, повышая плотность верхнего слоя атома и этим понижая егохимические свойства. Уменьшение хим. особенностей происходит по причине того, что убираются зазоры между элементарными частицами чуть ниже об этом напишу.
2) Часть элементарных частиц вылетают в окружающую атом среду. Наряду с этим происходит явление выделения тепла, энергии, поскольку вылетевшие из атома элементарные частицы влетают в соседние атомы и передают им собственную кинетическую энергию ( увеличивается температура, другими словами скорость перемещения атомов). Подобное явление увеличение температуры происходит и при ядерных реакция.
Сейчас механика
Заполним орбитали условными элементарными частицами.
Приобретаем картину:
Чистая геометрия. Размеры частиц условны, не учтено влияние температуры, но основное принцип понятен.
Чем больше зазоры, чем больше их количество, тем больше демпфирующие особенности атома, тем лучше химические особенности. Возможность того что фтор присоединит к себе другую молекулу существенно выше, чем возможность присоединения к атому Лития другого атома. От Лития всё отскакивает. К Фтору всё прилипает.
Чистая механика. Те элементы каковые находятся посередине смогут как отталкивать так и прилипать к вторым элементам в зависимости от того с каким элементом они реагируют. В случае если с Литием то прилипают (окисление), в случае если с фтором то отталкивают (восстановительные особенности).
Четыре состояния вещества.
1) Газообразное. В газообразном состоянии атомы имеют высокую скорость и отталкиваются от вторых атомов. Пролетают громадные расстояния до следующего столкновения.
Межмолекулярное расстояние громадно. Атомы постоянно находятся в движении. Межмолекулярное расстояние намного превышает размеры атомов.
2) Жидкое. Атомы движутся со средней скоростью, наряду с этим они всегда соприкасаются между собой. Полутвёрдое, полугазообразное состояние.
Межмолекулярное расстояние превышает размеры атомов, исходя из этого атомы смогут вольно перемещаться относительно друг друга, но уже имеется ограничения на стремительное перемещение из-за высокой плотности если сравнивать с газообразным состоянием.
3) Жёсткое. Атомы упорядочиваются в кристаллическую решётку. Межмолекулярное расстояние меньше диаметра атома. Атом ограничен в собственных перемещениях относительно атомов соседей.
Чтобы поменять место в кристаллической решётке атом обязан раздвинуть 2-3 атома соседа в один момент, что сделать отдельный атом неимеетвозможности, поскольку не имеет запаса кинетической энергии.
4) Плазма. Атомы имеют энергию и высокую скорость. Межатомная среда заполнена осколками атомов из-за нередкого сотрудничества их между собой.
Прекрасно излучает тепловую энергию, снова же из-за наличия стремительных осколков атомов.
5) Пока не открыто. Наполнен элементарными частицами, каковые появились по окончании распада атомов на составные части. Скорость частиц маленькая.
шанса и Энергии возможности для образования атома водорода не хватает, по причине того, что возможность объединения частиц в первое устойчивое состояние с заданным радиусом не хватает. Масса всех частиц однообразна. Скорость однообразна.
Энергия однообразна. Это связано с тем, что частицы всегда обмениваются ударами и этим уравнивают собственную энергию.
Химические связи.
Железная сообщение. Обрисована чуть выше в абзаце про жёсткое состояние вещества. Атом в кристаллической решётке держат атомы соседи, каковые ограничивают собственными размерами выход этого атома из собственной клетки в кристаллической решётке.
Ковалентная и частный случай ионная. Появляется при соударении атомов, которыми владел к различным валентным группам таблицы Менделеева. Связана со структурой внешнего слоя ядра атома.
Обрисовано чуть выше.
Понятная аналогия.
Атомы первой валентной группы отталкивают все остальные атомы, за счёт плотной структуры внешнего слоя атома. Аналогия — железный шарик. (Na)
Атомы 7 валентной группы — демпфируют удары вторых частиц и тем самым оставляют другие атомы около себя, поглощая их кинетическую энергию. Аналогия — пушистый игрушечный мягкий шарик. (Cl)
Обрисуем сотрудничество шариков.
1) Два железных шарика при ударе отскочат друг от друга. Химической реакции не случилось (Na+Nа).
2) Два мягких пушистых шарика при соударении образуют непрочное соединение. Их легко поделить, поскольку имеется прослойка воздуха между ними. (Cl2)
3) Железный шарик при соударении с мягким игрушечным шариком, застрянет, всячески запутавшись в нём. Сильная ковалентная сообщение. (NaCl).
Думаю сейчас ясно.
Если не светло возможно привести аналогии по сотрудничеству жёсткого упругого танка и мягкой податливой иномарки, дабы всем до конца было ясно.
Из-за чего валентных групп 8.
Это условное число. Оно просто характеризует степень заполнения внешней орбитали атома. Возможно было бы выразить его в процентах ничего бы не изменилось.